Ответы на вопрос:
ответ: 77,68%
дано:
m(caco₃) = 1 кг
m(пр.cao) = 0,435 кг
знайти:
η(сао)-?
объяснение:
м(сасо₃) = 0,1 кг/моль
n(caco₃) = m/m = 1 кг/0,1 кг/моль = 10 моль
m(cao) = 0,056 кг/моль
сасо₃ = сао + со₂
з рхр бачимо, що n(cao)=n(caco₃)
n(теор.cao) = 10 моль
n(пр.сао) = 0,435 кг/0,056 кг/моль = 7,768 моль
η(сао) = n(пр.сао)/n(теор.cao)*100%
η(сао) = 7,768/10*100% = 77,68%
відповідь: 77,68%
Метод электронного баланса:
1. Пишем степень окисления для каждого элемента сверху. (Показано на фото.)
2. Определяем окислительно-восстановительные процессы:
- Потеря электронов это окисление;
- Получение электронов это восстановление.
2N(+2) + 4e → 2N2(0) - восстановление
4N(+2) - 4e → 4N(+3) - окисление
Пишем количество электронов и сокращаем:
4 | 1
4 | 1
Значит, N2 используется 1 моль. Общая реакция:
6NO + 4KOH → 4KNO2 + N2 + 2H2O
NO является и окислителем, и восстановителем.
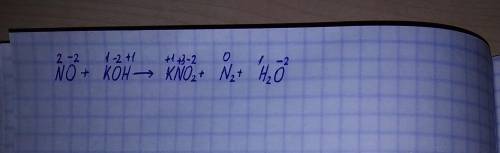
Популярно: Химия
-
Осуществить цепочку превращений...
 СуперТрололо25.04.2022 11:49
СуперТрололо25.04.2022 11:49 -
Какое из этих металл, кислород 2) водород, хлор 3) водород, кислород 4) металл,...
 palnikov200027.05.2023 14:52
palnikov200027.05.2023 14:52 -
вещество X массой 4,34 г сожгли в токе кислорода, в результате образовалось...
 Nikita2033012.12.2020 09:12
Nikita2033012.12.2020 09:12 -
Сравните строение электронной оболочки атомов а)кислорода и серы б)натрия...
 егормицевич23.10.2021 07:35
егормицевич23.10.2021 07:35 -
Ссамостоятельной с 7 вопроса до 10...
 vasilyukandrey30.05.2022 16:55
vasilyukandrey30.05.2022 16:55 -
41 по известной цепи днк достроить цепь; найти длину; рассчитать количество...
 belkairi10.08.2022 03:01
belkairi10.08.2022 03:01 -
Написать цепочку пропан - пропен - 2 хлорпропан хлорпропан- гексан...
 данил208010.09.2022 10:24
данил208010.09.2022 10:24 -
Сколько литров(н.у) газа останется в избытке при взаимодействии 3г водорода...
 кира63108.02.2022 12:14
кира63108.02.2022 12:14 -
Определите ситуацию, в которой 2co + o2 = 2co3 снижает равновесие...
 alesaastudinap0dbun16.06.2023 17:46
alesaastudinap0dbun16.06.2023 17:46 -
Определите массу(г) озона количеством вещества 1 моль...
 linakovtunenko105.04.2020 13:11
linakovtunenko105.04.2020 13:11
