Какая масса формалина с массовой долей формальдегида 40 процентов может образоваться если использовать альде гид, полученный при катали ти че с ко м окислении метана объемом 336 л (н.у.) кислородом воздуха. выход продуктов в реакции окисления равен 60
209
358
Ответы на вопрос:
336 л х гch4 + o2 --> hcoh + h2o22,4 30х=336*30/22,4= 450 г450 г 100%у г 60%у= 450*60/100 = 270 гw= m(в-ва)/m(p-pa)0,4=270/m(p-pa)m(p-pa)= 675 г
Найдем количество молей водорода и кислорода в смеси, то есть, сколько моль веществ содержится в 1 моле смеси.
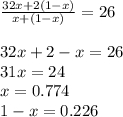
Выходит, что число молей кислорода равно 0.774 на 1 моль в смеси, а число молей водорода равно 0.226 моль на 1 моль смеси. Остается лишь умножить значения на 5, ведь спрашивается про 5 моль смеси.
n(O2)=0.774 * 5 = 3.87 моль
n(H2)=0.226 * 5 = 1.13 моль
При реакции водорода и кислорода образуется вода:
2H2 + O2 => 2H2O
Соотношение водорода и кислорода в реакции 2:1. 2 моля водорода на 1 моль кислорода. Выходит, что кислород в избытке. Считаем по водороду:
n¹(O2) = 0.5n¹(H2) = 0.565 моль
Все 1.13 моль водорода расходуются, вместе. сними уходит 0.565 моль кислорода. Значит, осталось еще:
3.87 моль - 0.565 моль = 3.305 моль кислорода.
Популярно: Химия
-
Задача з хімії ів! При нагріванні 25 г барій карбонату що містить 5% домішок...
 roma84501.09.2021 02:56
roma84501.09.2021 02:56 -
Напишите химичне ривняння между водой и киснем...
 Shaxrior21.06.2020 18:19
Shaxrior21.06.2020 18:19 -
При сгорании 14 г полиэтилена образуется углекислый газ объемом (н.у.) 1)...
 пецааааа102.11.2021 02:05
пецааааа102.11.2021 02:05 -
Составьте соответствующие химические формулы: BaO, SO, MgF, HS, FO, LiO....
 Harley29Davidson07.08.2020 05:04
Harley29Davidson07.08.2020 05:04 -
Уравнения реакций, при которых можно осуществить следующие превращения:...
 TMTEMI09.07.2020 00:50
TMTEMI09.07.2020 00:50 -
Ребят все три задания ...
 толик1414.06.2023 09:53
толик1414.06.2023 09:53 -
Какие из сульфидов ZnS, CdS, HgS осаждаются сероводором? Почему?...
 nrcsgt20.03.2022 13:21
nrcsgt20.03.2022 13:21 -
практическая работа по химии вариант 1 и таблица...
 Крис594231461312.09.2022 00:40
Крис594231461312.09.2022 00:40 -
Обчисліть кількість атомів Карбону в 0,25 моль стійкого органічного забруднювача,...
 PaPaDeDa29.12.2022 09:03
PaPaDeDa29.12.2022 09:03 -
Визначте максимальну кількість електронів, що міститься на 7s орбіталі....
 az34358strelok839017.01.2020 12:31
az34358strelok839017.01.2020 12:31
