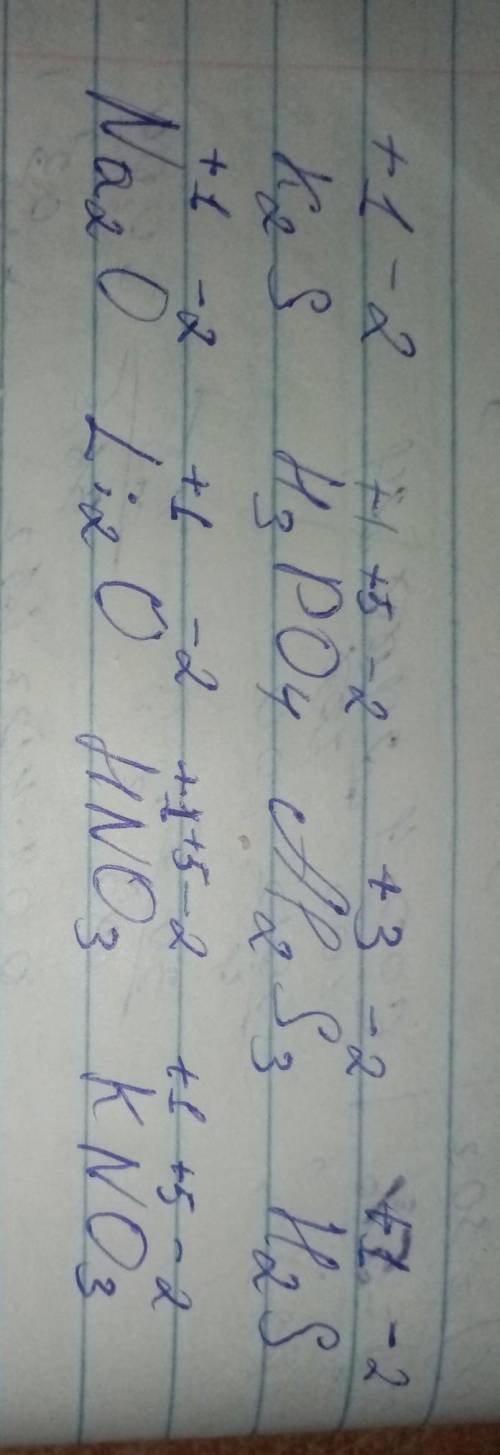Враствор объемом 378 см3 с массовой долей серной кислоты 12% и плотностью 1,08 г\см3 опустили кусочек цинка. рассчитайте массу выделевшегося водорода. h2so4 + zn = znso4 + h2 (у н2 стрелка вверх)
176
342
Ответы на вопрос:
49 х
zn+h2so4=znso4+h2
98 2
378 > 378 мл
1.08 г/см^3--> 1.08 г/мл
m(р-ра)=p*v=1.08*378=408.24 г
m(h2so4)=w(h2so4)*m(р-ра)=0.12*408.24=49 г
составляем пропорцию
49=х > 49*2 /98=1 г
98 2
ответ: m(h2) 1 г
Популярно: Химия
-
Заполните пропуски необходимыми словами, относящимися к данной эндотермической...
 namik14725836914.02.2020 13:50
namik14725836914.02.2020 13:50 -
1.Какие вещества являются а) гомологами б) изомеры 4,4 диметилпентин-2, метилциклобутен,...
 meskov07.05.2021 07:27
meskov07.05.2021 07:27 -
Рассчитайте pH буферного раствора который получится при сливании 100 мл 0,1...
 nastia0410201531.10.2020 05:58
nastia0410201531.10.2020 05:58 -
Какого цвета будет лаксус в розчене кислоты...
 Novikovavera8120.09.2020 21:44
Novikovavera8120.09.2020 21:44 -
під час згорання 5,6г кальцію утворилося 16 г речовини яка маса кисню була...
 22a03a198909.06.2022 00:37
22a03a198909.06.2022 00:37 -
Здійснити схему перетворення крохмаль - глюкоза - етаналь - оцтова кислота...
 kurilen28.02.2023 08:03
kurilen28.02.2023 08:03 -
Из перечисленных формул: н2s, k2so3, kon, so3, fe(oh)3, feo, n2o3, cu(po4)2,...
 accyxob24.02.2022 12:00
accyxob24.02.2022 12:00 -
Напишите уравнения реакций с которых можно осуществить следующие превращения:...
 Аминаgjdhkutdf17.09.2022 18:35
Аминаgjdhkutdf17.09.2022 18:35 -
Как из изопропила бензоата получить оксид углерода 4 c6h5-cooch(ch3)2+? =co2...
 HaGiNg18.04.2021 21:51
HaGiNg18.04.2021 21:51 -
Ch3-ch2-cooh + mg = ch3-ch2-cooh + br2 = ch3-ch2-cooh + ch3-ch2-ch2oh = ch3-ch2-cooh...
 ElinaN2829.07.2020 07:31
ElinaN2829.07.2020 07:31