Сколько молекул оксида углерода (IV) содержится в 1 мл этого газа при температуре 27°С и давлении 20 кПа?
Ответы на вопрос:
Дано:
CO₂
V = 1 мл = 1×10⁻⁶ м³
t = 27°C
p = 20 кПа = 20×10³ Па
Найти:
n(CO₂) - ?
1) Для нахождения молекул у оксида углерода (IV) используется формула Менделеева-Клайперона именно по такой формуле мы будем пользоваться:
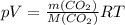 - Формула Менделеева-Клайперона
- Формула Менделеева-Клайперона
2) Из формулы Менделеева-Клайперона мы найдем массу оксида углерода (IV), но сначала мы найдем температуру в кельвинах, а потом его молекулярную массу:
T = t + 273 = 27 + 273 = 300 К
M(CO₂) = 12 + 16×2 = 12 + 32 = 44 гр/моль
m(CO₂) = (pV×M(CO₂))/RT = (20×10³ Па × 1×10⁻⁶ м³ × 44 гр/моль)/(8,31 Дж/(моль×К) × 300 К) = (2×10⁻² Дж × 44 гр/моль)/2493 Дж/моль ≈ 8,02×10⁻⁶ моль × 44 гр/моль ≈ 352,88×10⁻⁶ гр ≈ 3,5288×10⁻⁴ гр
3) Теперь находим количества вещества у оксида углерода (IV):
n(CO₂) = m(CO₂)/M(CO₂) = 3,5288×10⁻⁴ гр / 44 гр/моль = 8,02×10⁻⁶ моль
ответ: n(CO₂) = 8,02×10⁻⁶ моль
Решено от : 
Популярно: Химия
-
Запишите электронную конфигурацию и электронно-графическую формулу атома, ядро...
 milana0372milana07.10.2020 14:11
milana0372milana07.10.2020 14:11 -
Обчисліть швидкість реакції, якщо відомо, що концентрація речовини змінилася...
 karinayatskevioz1zkj13.08.2021 02:48
karinayatskevioz1zkj13.08.2021 02:48 -
Речовина (формула) Кремнезем Натрій хлории Фізична властивість речовини, характеристики...
 Tara880822.06.2021 07:22
Tara880822.06.2021 07:22 -
10. Медная пластина погружается в данный физиологический раствор: а) MgSO б)...
 rano0905.04.2020 21:57
rano0905.04.2020 21:57 -
Рассчитайте массовые доли химических элементов в веществе пентин-2...
 Marik1978200229.10.2021 20:42
Marik1978200229.10.2021 20:42 -
Сколько соли образуется в граммах при взаимодействии 44,8литроы аммиака (NH3)...
 Anastasia7wr22.07.2021 13:08
Anastasia7wr22.07.2021 13:08 -
Көмектесіңіздершіі өтііінііііш...
 kairatfylosof03.02.2020 05:31
kairatfylosof03.02.2020 05:31 -
Запишите уравнение реакции, с которых можно осуществить цепочку превращении CH2=CH2-CH3...
 СаняDots01.06.2020 08:45
СаняDots01.06.2020 08:45 -
Определите молекулярную формулу неизвестного соединения, состав которого состоит...
 ларисаяна09.03.2023 15:56
ларисаяна09.03.2023 15:56 -
Низькомолекулярні речовини що використовують для синтезу полімеру: а) ненасичені...
 loloshka56613.02.2021 15:28
loloshka56613.02.2021 15:28
