Cci , 3. Составьте уравнения реакций согласно предложенным схемам,
назовите образовавшиеся органические продукты:
а) бутадиен-1,3 + 2Br,
б) ацетилен + 2H,
в) бензол - HNO, Haso
4. Запишите уравнения химических реакций, соответствующих
схеме химических превращений:
Сн, Намах, ах,
-х,
Составьте структурные формулы веществ X, X, X, X, и назо-
NaOH
/етите
Но / Ha, POf x
вите их.
Ответы на вопрос:
3.
A)
CH2=CH-CH=CH2 + Br2 = Br-CH2-CH=CH-CH2-Br
дивинил + бром → 1,4-дибромбутен-2 / 1,2,3,4-тетрабромбутан
б)
CH=CH + 2H2 =Ni= CH3-CH3
ацетилен + 2·водород → (никель) → этан
CH=CH + H2 =Pd,H2SO4= CH2=CH2
ацетилен + водород → (палладий, сульфат бария) → этилен
в)
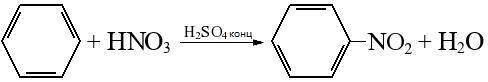
C6H6 + HNO3 =H2SO4(конц.)= H2O +
бензол + азотная кислота → (серная кислота конц) → нитробензол + вода
вот
Объяснение:
Окисно-відновні реакції — реакції, які супроводжуються переходом електронів від одних атомів, молекул або іонів до інших при зміні ступеня окиснення елементів. Речовину, що містить елемент, який віддає електрони, називають відновником. Процес віддачі електронів, при якому ступінь окиснення елемента зростає, називають окисненням. Речовину, що містить елемент, який приєднує електрони, називають окисником. Процес приєднання електронів називають відновленням. При відновленні ступінь окиснення елемента знижується. Ступінь окиснення елемента — це той електричний заряд атома цього елемента у сполуці, який розраховується, виходячи з припущення, що сполука складається з іонів. Або це той умовний заряд, який мав би атом елемента у сполуці при повному переході електронних пар, які утворюють зв’язок, до більш електронегативних атомів. Процеси окиснення та відновлення проходять одночасно і загальне число електронів, відданих відновником, дорівнює числу електронів, прийнятих окисником. У загальному вигляді О.-в.р. можна записати так: Am + Bp → Am-n + Bp+n, де: відновник: Am — nē ↔ Am-n — процес окиснення відновника; окисник: Вр + nē ↔ Bp+n — процес відновлення окисника.
Популярно: Химия
-
Вычислить объём воздуха необходимый для сжигания 10-литров метана...
 24566703.05.2020 01:25
24566703.05.2020 01:25 -
Составить цепочку реакций: алканы→алкены→спирты→альдегиды→карбоновые...
 sevara22106.05.2022 20:55
sevara22106.05.2022 20:55 -
Сколько граммов йода и спирта надо взять для приготовления 300г 10%...
 evamayninger2021.08.2020 05:14
evamayninger2021.08.2020 05:14 -
Na2so3+s4o2=na2so3+so2 ; данные na2so3- 64,2 кг , 16,3% найти массу...
 школьник81409.10.2020 21:00
школьник81409.10.2020 21:00 -
Нужно придумать с народным хозяйством или медициной. !...
 milka2018225.04.2020 11:06
milka2018225.04.2020 11:06 -
Скільки літрів сірчистого газу виділиться при взаємодії 1280г міді...
 Madwoman1715.05.2020 13:26
Madwoman1715.05.2020 13:26 -
В каких соединениях есть элементы с равными массовыми долями? Примите...
 Do1git27.05.2022 08:26
Do1git27.05.2022 08:26 -
Масса карбида кальция, необходимого для получения 20,04 л. ацетилена...
 Будина0511.03.2020 07:20
Будина0511.03.2020 07:20 -
Конспект о природных источниках углеводородов на 140+ слов...
 lida11303.01.2022 20:50
lida11303.01.2022 20:50 -
вычислите массу карбоната кальция, если в результате реакции взаимодействия...
 oobostoo02.06.2023 01:34
oobostoo02.06.2023 01:34
