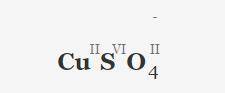Ответы на вопрос:
Cu + 4hno3 = cu(no3)2 + 2no2 +2h2o 1.вычисляем, ск. чистой меди прореагировало: 100% - 35% = 65% . это 3,2 х 65 : 100 = 2,08 г чистой меди. 2.вычислим, сколько теоретически должно выделиться оксида азота из 2,08 г меди: 1 моль меди = 64 г, след. , 2,08 г меди составляют 2,08 : 64 = 0,0325 моля. на 1 моль меди выделяется 2 моля оксида азота, след. , на 0,0325 моля меди получится 2 х 0,0325 = 0,065 моля no2. в граммах это будет: 46 г (1 моль no2) х 0,065 = 2,99 г no2.(теоретически) . 3. теперь считаем, какой выход оксида азота получился от теоретического: 2,99 г 100% выход; 1,3 г х% х = 1,3 х 100 : 2,99 = 43,48%
Популярно: Химия
-
Рассчитайте массу кислорода, необходимое для сжигания метана с содержанием вещества...
 krejzin02.10.2020 14:16
krejzin02.10.2020 14:16 -
3. При растворении 10 грамм технического цинка в избытке разбавленной соляной кислоты...
 Дисконет04.02.2021 03:42
Дисконет04.02.2021 03:42 -
Осуществить превращения. Реакции ионного обмена составить в полном и сокращенном...
 valuchska05.10.2020 15:11
valuchska05.10.2020 15:11 -
Общими формулами высшего оксида, высшего гидроксида и летучего водородного соединения...
 ksenia23110629.12.2022 12:12
ksenia23110629.12.2022 12:12 -
Екі элемент химиялық жолмен біріккенде қандай таза зат түзіледі? ерітінді элемент...
 Aseka0910.04.2023 11:07
Aseka0910.04.2023 11:07 -
Менделеев бұрын Ким болған?...
 Палина20041305.12.2021 17:45
Палина20041305.12.2021 17:45 -
3. Ағыс жылдамдығы 2 м/с өзенде катер жағаға қатысты 3,5 м/с жылдамдықпен перпендикуляр...
 Soffa611026.04.2020 09:56
Soffa611026.04.2020 09:56 -
Знайти масову частку натрій...
 katrin0506920.09.2021 06:32
katrin0506920.09.2021 06:32 -
В схеме генетического ряда серы S → SO2 → X формула пропущенного вещества Х − это...
 belka2005527.03.2023 10:05
belka2005527.03.2023 10:05 -
Физикалық дене стаканды қандай химиялық заттардан жасауға болады?...
 smail13012.04.2023 20:30
smail13012.04.2023 20:30