При сгорании 11,6 г газообразующего углеводорода образовалось 35, 2 г углекислого газа и 18г воды. плотность газа по водороду равна 29 найти молекулярную формулу вещества. сколько это будет стоить?
133
224
Ответы на вопрос:
cxhy+o2=co2+h2o
n(co2)=35.5/44=0.8
n(h2o)=18/18=1
считаем по недостатку,т.е по углекислому газу,значит n(cxhy)=0.8 =>
m(cxhy)=11.6/0.8=14.5
так как его плотность по водороду 29,найдём малекулярную массу искомого: 29х2=58
58/14.5=4
c4h10
Степень диссоциации 75%
Объяснение:
Степень диссоциации показывает какая часть всех молекул продиссоциировала на ионы.
Степень диссоциации равна отношению числа распавшихся на ионы молекул к общему числу молекул и выражается в процентах:
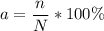 , где a - степень диссоциации, n - число распавшихся на ионы молекул, N - общее число молекул.
, где a - степень диссоциации, n - число распавшихся на ионы молекул, N - общее число молекул.
По условию: n = 150; N = 200.
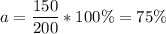
Степень диссоциации 75%
Популярно: Химия
-
1. Составьте уравнения тех реакций, которые протекают практически до конца,...
 умник162д15.03.2022 13:21
умник162д15.03.2022 13:21 -
3. Составьте формулу нитрата серебра (1) по массовым долям элементов: w(Ag)...
 Кица23404.08.2020 03:30
Кица23404.08.2020 03:30 -
Какое из веществ, формулы которых приведены ниже, является основанием? 2(4)3...
 sachaice02.01.2023 06:20
sachaice02.01.2023 06:20 -
2. Рассчитайте массовые доли элементов соединения ZnSO4 сульфата цинка. ответ:...
 cat000000018.04.2022 16:36
cat000000018.04.2022 16:36 -
Составьте молекулярное, полное и сокращенное ионное уравнения реакции. 1....
 tushenka8812.03.2022 20:03
tushenka8812.03.2022 20:03 -
Томендеги тизиммен заттар мен денеледи болип жаз: муз кесеги, ас тузы, кайшы,...
 Clook202302.01.2022 08:17
Clook202302.01.2022 08:17 -
Сынауыққа мырыштың бір түйірін салып, үстіне бірнеше -актX AHAыі Мырыштың...
 silina201819.06.2023 12:42
silina201819.06.2023 12:42 -
1.Складіть формули вуглеводнів які містять а) 44 атоми Карбону б) 72 атоми...
 Dispasito15.07.2022 01:52
Dispasito15.07.2022 01:52 -
Массовая доля серы в сульфите калия k2so4 равна решение (подробно)...
 sonyavolkova2619.06.2023 21:11
sonyavolkova2619.06.2023 21:11 -
Составьте на основе реакции нейтрализации,если известна масса одного из вступающих...
 Yasik22823.02.2021 02:11
Yasik22823.02.2021 02:11
