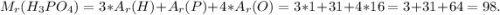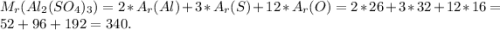Вычислите относительные молекулярные массы следующих соединений :H3PO4A12(S04)3
272
286
Ответы на вопрос:
Объяснение:
Mr(H3PO4) = 1*3 + 31 + 16*4 = 98
Mr(Al2(SO4)3 = 27*2 + 32*3 + 16*12 =342
Дано m(cao)=150 kg w(прим)=20% η=85% n(ca(oh) m(cao)=150-(150*20%/100%)=120 kg 120 x cao+h2o--> ca(oh)2 m(cao)=56 kg/kmol . m(ca(oh)2) = 74 kg/kmol 56 74 x=120*74 / 56 = 158.57 kg m(ca(oh)2)= 158.57*η / 100% = 158.57*85%/100%=135 kg n(ca(oh)2)=m(ca(oh)2) / m(ca(oh)2)= 135/74 = 1.82 kmol ответ 1.82 кмоль
Популярно: Химия
-
Решить . какова формула галогеноводорода, если смесь данного галогеноводорода...
 kristka9814.09.2022 05:14
kristka9814.09.2022 05:14 -
Какие металлы средней активности реагируют с водой при повышенной температуре,...
 Dashuli4ka200121.02.2021 21:02
Dashuli4ka200121.02.2021 21:02 -
Скакими неметаллами реагируют активные металлы при нагревании?...
 pershikovanata22.05.2022 08:39
pershikovanata22.05.2022 08:39 -
Как ориентироваться в свойствах заряда ядра по таблице менделеева?...
 Стары16.02.2023 10:09
Стары16.02.2023 10:09 -
Как ориентироваться в свойствах энергии связи по таблице менделеева? обьясните...
 ruzar198721.05.2021 19:53
ruzar198721.05.2021 19:53 -
Решить ланцуг caco3- cao- ca(oh)2- ca3(po4)2...
 nadiacolupaeva09.03.2020 06:54
nadiacolupaeva09.03.2020 06:54 -
При взаимодействии 16 г серы с необходимым количеством серной кислоты образовался...
 Vanysik22.11.2022 11:28
Vanysik22.11.2022 11:28 -
Определите массу борной кислоты, которую нужно растворить в 500 мл, чтобы...
 02vopros0229.12.2021 20:41
02vopros0229.12.2021 20:41 -
С. мне нужно , последние уроки , не нахватать двоек)...
 murad209712.02.2023 18:42
murad209712.02.2023 18:42 -
Рассчитайте массу воды и хлорида натрия, необходимые для приготовления 0,05...
 10RAM1020.09.2021 01:05
10RAM1020.09.2021 01:05