5. Обратимая реакция выражается уравнением 2SO2 + O2 ↔ 2SO3. В момент равновесия кон¬цент¬рации веществ были: [SO2]=0,02моль/л; [О2]=0,04моль/л; [SO3]=0,03 моль/л. Вычислите значе¬ния константы химического равновесия и исходные концентрации кислорода и оксида серы (IV).
130
145
Ответы на вопрос:
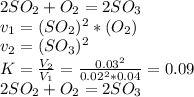
2моль -1 моль-2 моля
расходы : если получено 0,03 моль SO3, для получения такого количество SO3 , в реакции тратится 0,03 моль SO2 и 0,015моль кислорода: 0,03:2=0,015
Объяснение:
Дано: m(p-pa hcl) = 146 r ω(hcl) = 20% или 0,2 найти: v( решение. m(hcl) = m(p-pa hcl)×ω(hcl) = 146 г*0,2 = 29,2 г m(hcl) = 36,5 г/моль n(hcl) = m(hcl)/m(hcl) = 29,2 г/36,5 г/моль = 0,8 моль vm = 22,4 л/моль мg + 2hcl = mgcl2 + h2↑ из ухр видно, что n(h2)=0,5n(hcl) n(h2)= 0,5×0,8 моль = 0,4 моль v(h2) = n(h2)×vm = 0,4 моль×22,4 л/моль = 8,96 л ответ: 8,96 л
Популярно: Химия
-
(Нужны только ответы) ( ) 5. З яких речовин можна добути кисень...
 ЮраУтюг14.01.2022 01:57
ЮраУтюг14.01.2022 01:57 -
1) В какой клетке дано определение понятия «Аллотропия»? 2)...
 пучкаек04.10.2020 04:05
пучкаек04.10.2020 04:05 -
8. Электронная конфигурация внешнего электронного слоя кальция:...
 кал1231.12.2020 02:08
кал1231.12.2020 02:08 -
(Нужны только ответы) ( ) 1. Вкажіть рівняння реакції розкладу:...
 stashea04.06.2023 11:04
stashea04.06.2023 11:04 -
Задача визначити, яка маса натрій нітратуутворюється при змішуванні...
 elvinsasylbaeva15.03.2023 16:16
elvinsasylbaeva15.03.2023 16:16 -
Наименьшими основными свойствами обладает Выберите один ответ....
 ванямна25.08.2022 10:39
ванямна25.08.2022 10:39 -
Вычислите массовую долю % оксида фосфора фосфора (V) в соли...
 Bossak08.04.2022 01:21
Bossak08.04.2022 01:21 -
Осуществить цепочку превращений: CH3-CHO-CH3-CH2-OH→HC=CH→CH3...
 Лия021122.05.2023 23:18
Лия021122.05.2023 23:18 -
переработки твердого топлива в основе, которого сжигание топлива...
 Mishcka1020007.04.2023 09:08
Mishcka1020007.04.2023 09:08 -
с химией Тема Окислительно-восстановительные реакции . Нужно...
 IraIvan20.07.2021 22:49
IraIvan20.07.2021 22:49
