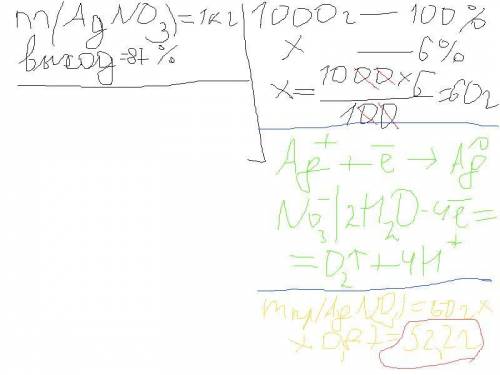Хелп!!!
1кг 6%-го раствора нитрата серебра подвергнут электролизу в течении 1 часа. выход по току составляет 87%. Запишите уравнения катодного и анодного процессов. Рассчитайте, какое количество электричества было пропущено через электролит
245
360
Ответы на вопрос:
11,2 г х л
с4h8 + 6 o2 = 4co2 + 4h2o
n = 1 моль n = 6 моль
mr = 56 г/моль vm = 22,4 л/моль
m = 56 г v = 134,4 л
11,2 г с4н8 - х л о2
56 г с4н8 - 134,4 л о2
v(o2) = 11,2 * 134,4 / 56 = 26,88 л
Популярно: Химия
-
На нейтрализацию смеси фенола и этанола затрачен раствор объемом 50 мл с массовой...
 sxxaaa05.01.2021 04:50
sxxaaa05.01.2021 04:50 -
Осуществите ряд превращений: ch4-ch3ci-c2h5br...
 Kinder164406.03.2020 08:03
Kinder164406.03.2020 08:03 -
11,2 г caо обработали 0,6 моль нno3. найти массу полученной соли, при 75% выхода...
 5312макс124520.06.2023 00:50
5312макс124520.06.2023 00:50 -
Напишите молекулярное и сокращенное уравнение реакции между растворами азотной...
 Pinkaktus25.11.2020 21:45
Pinkaktus25.11.2020 21:45 -
Тепловой эффект горения водорода = 571,6 кдж. найти объем сожженого водорода если...
 anastasiya25809.01.2022 12:37
anastasiya25809.01.2022 12:37 -
Визначити кількість речовини оксигену, що міститься в глюкозі (с6н12о6) масою...
 snezhanavasileozvjsv02.10.2020 09:08
snezhanavasileozvjsv02.10.2020 09:08 -
Чему равен температурный коэффициент вант-гоффа, если известно, что при понижении...
 KarenXacul8016.04.2022 18:24
KarenXacul8016.04.2022 18:24 -
Из 1,00 г анилина было получено 2,04 г n-бензоилфениламина c6h5nhcoc6h5. рассчитайте...
 ananaaaas1124.10.2020 22:31
ananaaaas1124.10.2020 22:31 -
Какую среду имеют водные растворы ацетата натрия, сульфата алюминия,карбит натрия?...
 minskaya8622.12.2021 15:02
minskaya8622.12.2021 15:02 -
Смешали 28 г 9%-ного и 25 г 31%-ного растворов гидроксида натрия. чему равна массовая...
 STIX718.08.2022 03:42
STIX718.08.2022 03:42