Найди сумму коэффициентов перед формулами веществ, в которых изменилась степень окисления цинка в ходе окислительно-восстановительной реакции, схема которой:
Zn+HNO3→Zn(NO3)2+NH4NO3+H2O.
2.Напиши уравнение химической реакции, протекающей при взаимодействии гидроксида натрия с хлоридом магния. Вычисли, чему равна сумма коэффициентов в уравнении этой химической реакции, и введи её в качестве ответа.
3.Напиши название оксида, который образован химическим элементом S(IV), и рассчитай его молярную массу.
4.Вставь в уравнение реакции пропущенный коэффициент: 4P+... O2=2P2O5
5.Напиши уравнение химической реакции, протекающей при взаимодействии гидроксида натрия с оксидом серы(IV). Вычисли, чему равна сумма коэффициентов в уравнении этой химической реакции, и введи её в качестве ответа
6.С какими из указанных веществ: CaO, Cu(OH)2, CO2, K2CO3 — не взаимодействует HNO3?.
Заранее
157
243
Ответы на вопрос:
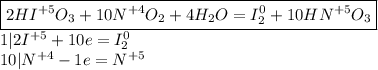
Йод - окислитель
Азот - восстановитель
Объяснение:
Запишем уравнение: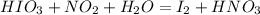
Расставим степени окисления: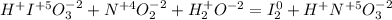
Оставим у тех что меняют степень окисления:
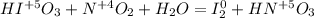
Составим баланс и уравняем: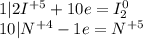
Йод - окислитель, восстановление (принимает электроны)
Азот - восстановитель, окисление (отдает электроны)
Следовательно перед йодом слева 2, чтобы уравнять с двухатомным нулевыми, перед азотами 10 и перед водой 4
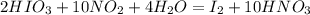
Популярно: Химия
-
Значение солей в жизни человека. напишите кратко ....
 урсвт11.02.2022 11:55
урсвт11.02.2022 11:55 -
Составить формулу : -3,3-диэтилпропан...
 николь4323.04.2022 03:07
николь4323.04.2022 03:07 -
Сколько молекул содержится в 180 мг воды?...
 заразарема06.01.2020 00:38
заразарема06.01.2020 00:38 -
Проеведите реакцию. k-k2o2-k2o-koh k2o-k2co3...
 MariCasanova16.10.2020 14:48
MariCasanova16.10.2020 14:48 -
Составьте структурную формулу углеводорода, у которого с атомами...
 gogoja12.07.2020 11:26
gogoja12.07.2020 11:26 -
Марганец образует соединения +2 +3 +4 +6 +7 составьте формулы его...
 vkjfnjkvd27.02.2020 06:50
vkjfnjkvd27.02.2020 06:50 -
Закінчи рівняння дисоціації літій нітрату LiNO3, указавши формули...
 livanatalya08.09.2021 10:00
livanatalya08.09.2021 10:00 -
Скільки треба взяти води щоб приготувати 200 г розчину з масовою...
 ibrohim327.08.2021 05:54
ibrohim327.08.2021 05:54 -
В 2 пробирки поместите 1-2 гранулы цинка и кусочки меди, прилейте...
 помогитееееее322.09.2021 21:51
помогитееееее322.09.2021 21:51 -
Будьте ласкаві розвяжіть задачу...
 lcjewfyjozo07530.08.2022 05:46
lcjewfyjozo07530.08.2022 05:46
