8) газ, полученный при сжигании сероводорода в избытке кислорода, прореагировал с 200мл 40%-го раствора гидроксид натрия с плотностью 1,43 г/см3 с образованием средней соли. найдите объём (л) сероводорода, израсходованного в реакции.
120
371
Ответы на вопрос:
2h2s + 3o2 --> 2so2 + 2h2o
so2 + 2naoh --> na2so3 + h2o
m(р-раnaoh)=500*1.28= 640 г
m(в-ваnaoh)=640*0.25= 160 г
n(naoh)=160/40 = 4моль
n(so2)= n(naoh)/2 = 4/2=2моль
n(so2)=n(h2s)=2 моль
v(h2s)=2*22.4=44.8 л
подробнее - на -
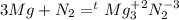 - нитрид магния
- нитрид магния
 - нитрид алюминия
- нитрид алюминия
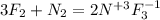 - фторид азота (III)
- фторид азота (III)
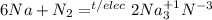 - нитрид натрия
- нитрид натрия
У исходных в-в степени окисления равны нулю
Популярно: Химия
-
III - значення відносної молекулярної маси цинк сульфату І П І І...
 20093926.03.2021 16:00
20093926.03.2021 16:00 -
Расположите элементы в порядке увеличения электроотрицательности...
 ЦУКПРОЛ16.11.2022 11:40
ЦУКПРОЛ16.11.2022 11:40 -
Змішали 145 г. розчину з масовою часткою кислоти 10% і 290 г розчину...
 nastich129.04.2022 06:16
nastich129.04.2022 06:16 -
1Назовите из перечня веществ электролиты BaCl2 CaO H2 SO4 Zn(OH)2...
 Dmitry023214110.07.2021 22:09
Dmitry023214110.07.2021 22:09 -
Какие вещества можно получить при окисления этаналя в различных...
 Muffs11.10.2020 04:07
Muffs11.10.2020 04:07 -
Яка маса негашеного вапна утвориться при згоранні 2грам кальцію...
 Meryem9828.04.2022 14:02
Meryem9828.04.2022 14:02 -
Вычислите объём СО2 (н. у.), который выделится при взаимодействии...
 Дима56677916.01.2022 20:31
Дима56677916.01.2022 20:31 -
Для взаємодії із сумішшю масою 5 г, яка містить етанол та фенол,...
 lev050580507.12.2020 21:39
lev050580507.12.2020 21:39 -
Нужна .какой объём углекислого газа ( норм. усл. ) образуется при...
 yakovlevakristi16.11.2020 17:24
yakovlevakristi16.11.2020 17:24 -
Схема строения атома cr(хром),ba(бария),mo(молютден)...
 Nazarova4304.06.2022 20:33
Nazarova4304.06.2022 20:33
