Вычислите объем воздуха,который потребуется для сжигания в 115г углерода содержащего 5% примесей.
234
368
Ответы на вопрос:
Пишем реакцию с условием что углерод сгорает до конечного продукта со2 c + o2 = co2 считаем массу чистого углерода m(c) = w*m(с с примесями) = 0.95*115 = 109.25 грам считаем количество вещества углерода n = m/m = 109.25/12 = 9.1 моль по уравнению реакции кислорода нужно тоже 9,1 моль считаем объем кислорода v = n*vm = 9.1*22.4 = 203.84 литра кислорода в воздухе 21% или 0,21 считаем объем воздуха v(воздуха) = v(кислорода)/φ = 203.84/0.21 = 970.67 литра ответ: 970,67 литра.
1. Г)МnO (V||
2B) CaCO3 .....+.....(реакция....);
3.На фотке трети задания
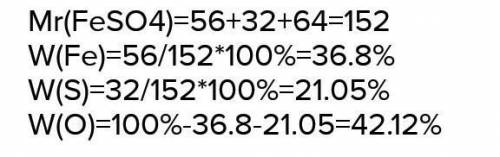
Популярно: Химия
-
Молекулярная формула: - уксусной кислоты и этанола -глицирина и глюкозы -аминоуксусной...
 sofia20000009.09.2022 05:28
sofia20000009.09.2022 05:28 -
Расскажите о структуре периодической таблицы элементов и поясните почему большие...
 lilofun20.07.2022 21:03
lilofun20.07.2022 21:03 -
Напишите уравнение реакций,соответствующих цепочке превращений : ацетилен⇒уксусный...
 фиксоня26.10.2022 05:19
фиксоня26.10.2022 05:19 -
Если смешать mno2 и h2o2, то получится 2h2o+ o2, mn02 не расходуется, т.к. катализатор....
 pughluy25.06.2020 09:56
pughluy25.06.2020 09:56 -
Определить массу меди ,полученную восстановление 320г оксида меди,если практический...
 dnlnv06.08.2020 05:55
dnlnv06.08.2020 05:55 -
35 ! мno2+2h2o - какая смесь? однородная?...
 daniilsemkin0507.01.2020 18:36
daniilsemkin0507.01.2020 18:36 -
Осуществить превращения по заданной схеме cuso4 - cu(oh)2 - cuo - cu реакции...
 Голес05.10.2022 17:47
Голес05.10.2022 17:47 -
Расположите элементы в порядке усиления неметалличности mg, ba, ca. объясните...
 Алёна11Кот14.10.2020 14:19
Алёна11Кот14.10.2020 14:19 -
Определите тип реакции (соединение, замещение, разложение, обмен) 1) К + H2 SO4...
 vladimir0004129.12.2021 02:54
vladimir0004129.12.2021 02:54 -
Дана схема окислительно - восстановительной реакции Составьте электронный баланс...
 KOTE42230.05.2020 06:44
KOTE42230.05.2020 06:44
