28,4 г оксида фосфора растворили в 200 г воды при нагревании. найдите массовую долю ортофосфорной кислоты в полученном растворе
280
384
Ответы на вопрос:
Переведем массу оксида фосфора в моль, разделив на молярную массу: 28.4/142 =0.2 теперь составим уравнение реакции гидролиза: p2o5 +3h2o =2h3po4 из этого уравнения мы видим, что фосфорной кислоты образовалось 0.4 моль, так как на 1 молль оксида фосфора образуется 2 моль фосфорной кислоты. теперь найдем массу фосфорной кислоты, умножив количество вещества на молярную массу: 0.4*98 =39.2 грамма. теперь разделим массу кислоты на массу раствора: 39.2/(200+28.4) =0.15 =15%
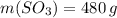
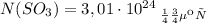
Объяснение:
Оксид серы (VI) - это соединение шестивалентной серы с кислородом, степень окисления которого как правило равна (-2) - т.е. SO3.
Всего у нас 5 моль SO3
Масса вещества равна произведению количества вещества на его молярную массу
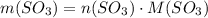
Вычислим молярную массу SO3:
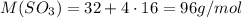
Найдем массу 5 моль SO3
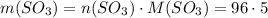
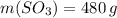
Количество молекул вещества равно произведению количества этого вещества на число молекул в 1 моль вещества (стандартное значение)
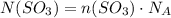
где
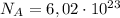
Отсюда:
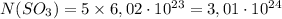
Популярно: Химия
-
баллов!!! МНЕ СКОРО СДАВАТЬ!!!! Чему равны масса, объём, количество вещества...
 Alips10.04.2020 17:24
Alips10.04.2020 17:24 -
Разделите данные список на оксид основание соли....
 Pinno4ka08.01.2022 03:28
Pinno4ka08.01.2022 03:28 -
Составте формулу кислот по известным кислотным остатком HxRy дайте нозвание...
 Tiggeri08.06.2022 19:51
Tiggeri08.06.2022 19:51 -
Элементтер буынының саны 5500 болатын полиэтилен макромалекуласының массасы...
 TheJurasikBint05.07.2022 01:57
TheJurasikBint05.07.2022 01:57 -
1. Кем и когда был открыт периодический закон? 2. Как изменяются металлические...
 BotanicPanik26.04.2023 16:21
BotanicPanik26.04.2023 16:21 -
Дайте ответ быстро Выполните тест «Соли» 1. Средняя соль 1)Na2SO4 2)NaHCO3...
 Mooz24.02.2020 15:21
Mooz24.02.2020 15:21 -
Урок по химии 8 класс Дата 19/05/20 Практическая работа «Решение экспериментальных...
 Hava99111120.06.2021 14:34
Hava99111120.06.2021 14:34 -
Для речовин якого класу сполук характерні подвійні зв’язки між атомами Карбону...
 lebedevamilp00sr927.04.2021 03:32
lebedevamilp00sr927.04.2021 03:32 -
25% водорода, содержащего 75% углеродов плотность 0.55...
 дира301.09.2020 08:20
дира301.09.2020 08:20 -
задание: приведите формулы 5-ти солей, молекулы которых образовались 6-ю...
 rubyrose200327.05.2020 01:31
rubyrose200327.05.2020 01:31
