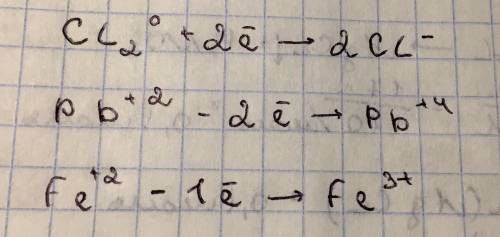Определите объем газа и массу соли, которая образуется при реакции 9,8 г серной кислоты с оксидом меди (ii)
212
320
Ответы на вопрос:
Сuo + 2h2so4(конц.) = cuso4 + so2 + 2h2o n(h2so4) = m(h2so4)/m(h2so4) m(h2so4) = 98 г/моль n(h2so4) = 9.8 г/98 г/моль = 0,1 моль из стехиометрических коэффициентов уравнения реакции следует, что n(cuso4)=n(so2)=1/2n(h2so4) = 0.05 моль m(cuso4) = 160 г/моль m(cuso4) = n(cuso4)*m(cuso4) = 0,05 моль*160 г/моль = 8 г vm = 22,4 л/моль v(so2) = n(so2)*vm = 0.05 моль*22,4 л/моль = 1,12 л ответ: 1,12 л; 8 г
Популярно: Химия
-
Отнш комектесндерш керек берем жаратылыстану 6 сынып...
 ArinaKappa06.05.2022 00:07
ArinaKappa06.05.2022 00:07 -
Позначте химичиними символами а)Атом Гідрогену.б)Два атоми Гідрогену.в)...
 лиза471021.06.2020 09:59
лиза471021.06.2020 09:59 -
Су мен тұз қоспаның түрі өтініш быстыра...
 rostikptashnik17.11.2022 17:48
rostikptashnik17.11.2022 17:48 -
S→SO²→SO³→H²SO⁴→CaSO⁴...
 hdjeugwcwtixuvbekz13.06.2020 11:21
hdjeugwcwtixuvbekz13.06.2020 11:21 -
Определить объем водорода образовагшегося при взаимодейстии 6,5г...
 denisdudkin73911.05.2022 03:48
denisdudkin73911.05.2022 03:48 -
Розрахуйте концентрації іонів водню та гідроксид-іонів в розчині...
 Mirano200426.01.2022 08:24
Mirano200426.01.2022 08:24 -
Күкірттің атомдық массасы қандай тауып беріңіздерш...
 Никита1111111495755818.06.2023 22:39
Никита1111111495755818.06.2023 22:39 -
, ответьте по химии очень...
 12345644524.10.2022 03:18
12345644524.10.2022 03:18 -
написаит уравнения реакций, с которых можно осуществить превращения:...
 matisina4815.08.2020 13:51
matisina4815.08.2020 13:51 -
Химия, уравнения реакций Составьте уравнения реакций, с которых...
 леракулдошина30.10.2021 01:10
леракулдошина30.10.2021 01:10