Вычислите массу и объём водорода,который образуется при взаимодействии цинка с 73 г. соляной кислоты.
105
383
Ответы на вопрос:
Zn + 2hcl = zncl2 + h2 m(hcl) = 36.5 г/моль n(hcl) = 73/36.5 = 2 моль n(h2) = n(hcl) / 2 = 1 моль v(h2) = 1 * 22.4 = 22.4 л m(h2) = 2 г/моль n(h2) = 1 *2 = 2 г
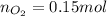
Объяснение:
Запишем уравнение реакции (сжигание натрия):
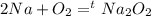
Согласно стехиометрическому закону количество вещества натрия и кислорода относятся также как коэффициенты в реакции:
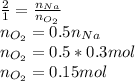
Популярно: Химия
-
Решить цепочку превращений,показать молекулярное и ионное уравнение сa(oh)2-cacl2-caco3...
 VaryaStar5523.09.2022 12:27
VaryaStar5523.09.2022 12:27 -
Определите валентность элементов в окислах: li2o. feo. fe2o3. mgo. pbo2. mno2....
 kisilevars200328.12.2021 11:07
kisilevars200328.12.2021 11:07 -
Дать характеристику 2 любых элементов 1 метал, другой не металл!...
 алсу15030.03.2022 08:47
алсу15030.03.2022 08:47 -
Найти коэффициенты fecl3+ki fecl2+i2...
 anaw8111.03.2023 17:11
anaw8111.03.2023 17:11 -
Осуществите цепочку ca-cao-ca(oh2)-caco3-cao...
 Jyrtasa19.01.2023 23:02
Jyrtasa19.01.2023 23:02 -
Осуществите превращение алюминий-гидроксид алюминия-оксид алюминия-сульфат алюминия-гидроксид...
 ХлойкаПрайс08.05.2023 07:00
ХлойкаПрайс08.05.2023 07:00 -
Дано: n(m2s)=0.6 моль найти: массу,объем...
 vitalik231203109.11.2020 12:44
vitalik231203109.11.2020 12:44 -
Закончите уравнения реакции,записать в ионном виде koh+h2so4— fe(oh)2+hno3—...
 lolipop172006.05.2021 09:26
lolipop172006.05.2021 09:26 -
Сумма коэффицентов в реакции ,схема которого ai+naoh+h2o-- nаaio2+h2...
 Сабина1409040292992910.02.2023 10:12
Сабина1409040292992910.02.2023 10:12 -
Найдите число атомов кислорода в порции газа объёмом ( н. у.) o2 33,6 дм кубических...
 вввв3107.10.2022 22:25
вввв3107.10.2022 22:25
